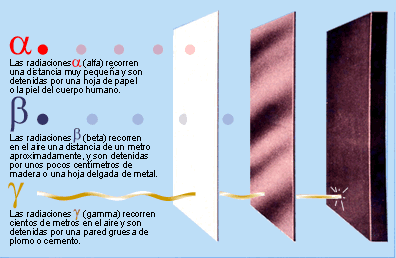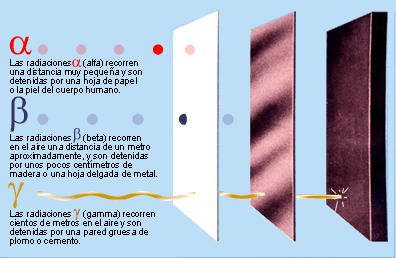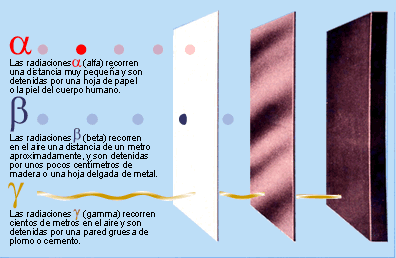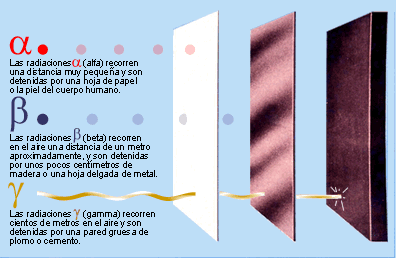
Elementos radioactivos
Actinio:
Es un metal que brilla en la oscuridad, produce una luz
azul, debido a su alta radiactividad. Posiblemente,
puede ser usado en el futuro para tratamientos médicos de enfermedades como el
cáncer, aun se estudia la posibilidad. Su número atómico es 89, su masa
atómica corresponde a 227 u, tiene como símbolo atómico Ac, el punto de fusión
es 1050° C y el de ebullición 3198° C.
Ástato:
Es el halógeno más pesado y uno de los elementos químicos más
extraños, también se le conoce como ástato. Su número atómico es 85, su masa
atómica corresponde a 208.9824, tiene como símbolo atómico At, el punto de
fusión es 254° C y el de ebullición 962° C.
Americio:
Es un metal inventado, no descubierto. Es de color plateado
y tonos blancos, pero pierde su brillo al tener contacto con el aire a
temperatura ambiente. Su número atómico es 95, su masa atómica corresponde a
243 u, tiene como símbolo atómico Am, el punto de fusión es 1176° C y el de
ebullición 2607° C.
Berkelio:
En su estado de metal, se
oxida con mucha facilidad, lo hace rápidamente al tener contacto con el aire o
el oxígeno a alta temperatura, es de color plateado y brillante, Este es un
elemento sintético, no se halla en la naturaleza. Su número atómico es 97, su
masa atómica corresponde a 247 u, tiene como símbolo atómico Bk, el punto de
fusión es 1050 °C y el de ebullición se desconoce.
Curio:
Es un maleable muy toxico, que entrar al cuerpo se dirige a
los huesos y su radiación no permite la formación de glóbulos rojos. Es un
elemento sintético. Su número atómico es 96, su masa atómica corresponde a 247
u, tiene como símbolo atómico Cm, el punto de fusión es 1340° C y el de
ebullición 3110° C.
Einstenio:
Es un metal sintético. Su número atómico es 99, su masa
atómica corresponde a 252 u, tiene como símbolo atómico Es, el punto de fusión
es 860 ° y el de ebullición 996 °C.
Fermio:
Se trata de otro actínido,
aun no tiene una forma metálica y es uno de los elementos químicos más pesados.
Su número atómico es 100, su masa atómica corresponde a 257 u, tiene como
símbolo atómico Fm, el punto de fusión es 852 °C y el de ebullición se
desconoce.
Francio:
Es el segundo elemento más escaso en la tierra, el metal
alcalino más pesado y el más pesado de los 101 primeros elementos de la tabla
periódica. Su número atómico es 87, su masa atómica corresponde a 223 u, tiene
como símbolo atómico Fr, el punto de fusión es 27° C y el de ebullición 677° C.
Lawrencio:
Es un elemento químico artificial, solo se halla de manera artificial
y en cantidades muy pequeñas. Su número atómico es 103, su masa atómica
corresponde a 262 u, tiene como símbolo atómico Lr, el punto de fusión es 1627°
C y el punto de ebullición se desconoce.
Mendelevio:
Su número atómico es 101, su masa atómica corresponde a 258
u, tiene como símbolo atómico Md, el punto de fusión es 827° C y el de
ebullición se desconoce.
Neptunio:
Es el metal más denso de los actínidos y el quinto de los
elementos naturales. Su número atómico es 93, su masa atómica corresponde a 237
u, tiene como símbolo atómico Np, el punto de fusión es 644° C y el de
ebullición 3900° C.
Nobelio:
Es sintético, sobre este elemento químico se sabe muy poco.
Su número atómico es 102, su masa atómica corresponde a 259 u, tiene como
símbolo atómico No, el punto de fusión es 827° C y el de ebullición se
desconoce.
Plutonio:
En su presentación de metal posee un color plateado y
brillante, se oxida velozmente al contacto con el iré, toma un color verdes y
amarillo opaco. Es sintético. Su número atómico es 94, su masa atómica
corresponde a 244 u, tiene como símbolo atómico Pu, el punto de fusión es 639°
C y el de ebullición: 3232° C
Polonio:
Es un metaloide difícil de encontrar, en acido fluido se
disuelve. Su número atómico es 84, Su masa atómica corresponde a 208.9824 u,
tiene como símbolo atómico Po, el punto de fusión es 254° C y el punto de
ebullición 962° C. Es importante porque se usa en la producción de neutrones, para también usarse en
eliminadores de estática.
Protactinio:
Es un metal, tiene una gran densidad y es un superconductor,
formar compuestos es su reacción con los compuestos como el oxígeno, el vapor
de agua y los ácidos inorgánicos. Naturalmente se produce en la corteza
terrestre. Su número atómico es 91, su masa atómica corresponde a 231,03588 u,
tiene como símbolo atómico Pa, el punto de fusión es 1840° C y el de ebullición
4027° C. Es importante porque su comportamiento químico en solución acuosa se
asemeja al del tántalo y del niobio más que al de los otros actínidos.
Radio:
Es muy peligroso; solo la inhalación, puede traer como
consecuencia problemas de salud, cáncer u otros trastornos. Es un elemento natural
que se encuentra en minerales de la naturaleza, arenas y también en algunos
lagos. Su número atómico es 88, su masa atómica corresponde a 226,0254 u, tiene
como símbolo atómico Ra, el punto de fusión 700° C y el punto de ebullición
1737° C.
Radón:
Es el último gas noble en la tabla periódica. Es pesado e
inerte. Su número atómico es 86, su masa atómica corresponde a 222 u, tiene
como símbolo atómico Rn, el punto de fusión es 71° C y el de ebullición -62° C.
Torio:
Su número atómico es 90, su masa atómica corresponde a
232,0381 u, tiene como símbolo atómico Th, el punto de fusión es 2028° y el de
ebullición 5061° C. Es importante porque se encuentra en casi cualquier lugar
de la tierra
Uranio:
Es un metal, que puro es maleable, fuertemente
electropositivo y algo paramagnético, pero es un mal conductor eléctrico. Su
número atómico es 92, su masa atómica corresponde a 238.02891 u, tiene como
símbolo atómico U, el punto de fusión es 1132° C y el punto de ebullición:
4131° C. El uranio es muy importante porque es el combustible nuclear más
importante.